

摘要:剖宫产子宫瘢痕妊娠(CSP)是妊娠囊着床于剖宫产子宫切口瘢痕处的一种特殊部位的异位妊娠。 若 CSP未经恰当的诊疗,可导致大出血、子宫破裂等危及生命的并发症,严重影响患者的生育力及身心健康。 虽然 CSP的治疗方式多样,但临床实践中仍缺乏被临床广泛应用的共识或指南来指导最佳治疗方案的选择。 近年来瘢痕妊娠的分型诊治越来越受重视。 瘢痕妊娠实用临床分型在山东省已得到较广泛的验证,针对每种类型推荐最佳治疗方案,治疗效果可靠,具有较高的临床应用价值。 因此,本专家组结合近年积累的临床经验及最新的临床研究结果,在实用临床分型诊治策略基础上,制定关于 CSP 分型诊治的专家共识,以期规范临床诊疗行为,指导临床工作。
关键词:剖宫产子宫瘢痕妊娠;异位妊娠;临床分型;治疗;专家共识
剖宫产子宫瘢痕妊娠(cesarean scar pregnancy,CSP),又称为剖宫产子宫瘢痕异位妊娠( cesareanscar ectopic pregnancy, CSEP),简称瘢痕妊娠,是指受精卵着床于剖宫产子宫切口瘢痕处的一种特殊类型的异位妊娠,属于剖宫产术的一种远期并发症。本文仅包括妊娠≤12 周的 CSP。 近年来,世界范围内 CSP 的发病率呈上升趋势,由于我国较高的剖宫产率,CSP 发病率较高。若 CSP 没有得到恰当的诊治,可导致危及生命的大量子宫出血、子宫破裂,甚至子宫切除术等严重2 山 东 大 学 学 报 (医 学 版) 61 卷 11 期并发症的发生,严重影响患者的生育力及身心健康。为了指导 CSP 的规范诊治,中华医学会于 2016 年更新并发布了《剖宫产术后子宫瘢痕妊娠诊治专家共识》。 2020 年美国母胎医学会 ( Society forMaternal⁃Fetal Medicine, SMFM) 综合文献,制定了《#49:剖宫产瘢痕妊娠指南》,并于 2022 年更新发布了《 #63:剖宫产瘢痕妊娠指南》。 这些国内外共识及指南对 CSP 的诊治具有重要的临床指导意义,但仍不能满足实际临床应用,迫切需要能够被临床广泛应用的共识或指南来指导个体化、最佳治疗方案的选择。研究表明,CSP 的临床类型不同,大出血风险及预后存在差异,准确的临床分型系统有助于指导选择最佳的治疗方案。 然而,以往的分型系统所采用的超声指标比较宽泛,并没有针对每一类型提出具体的临床治疗方案。 近年来,我省所推行的基于瘢痕妊娠实用临床分型对 CSP 进行详细分型,并针对每种类型推荐了最优手术治疗方案,临床治疗效果可靠,具有较高的临床应用价值。 因此,本专家组结合今年积累的临床经验及最新的临床研究结果,在实用临床分型诊治策略以及上述共识和指南的基础上,制定此关于 CSP 分型诊治的专家共识,以期规范临床诊疗行为,指导临床工作。
1 CSP 的发病机制
CSP 的病因尚不清楚,推测可能由于剖宫产术后子宫切口愈合不良,瘢痕部位形成微小裂隙,宫腔微环境受宫腔操作、宫腔粘连等因素影响不利于受精卵种植,或受精卵发育迟缓或运行过快,通过微小裂隙进入子宫肌层而着床。 由于瘢痕处肌层薄弱并纤维化,随着妊娠继续孕囊增大,有可能发生瘢痕处破裂、大出血、胎盘植入性疾病(placenta accretaspectrum, PAS)甚至危及母胎生命等风险。 研究显示,CSP 与 PAS 具有相似的发病过程,CSP 继续妊娠将发展为 PAS,提示 CSP 是 PAS 的先期病变,二者属于同一疾病的不同发展阶段。 病理学发现两者均有绒毛浸润至瘢痕肌层组织内、蜕膜变薄或缺失。研究表明,CSP 发生的高危因素包括臀位剖宫产、距前次剖宫产小于 2 年。 剖宫产史虽然是 CSP 发生的前提条件,但剖宫产次数增多并不增加 CSP 的风险。 虽然研究认为子宫切口双层缝合与单层缝合相比,有利于增加瘢痕处残余肌层的厚度,可能会减少 CSP 的发生率,但是子宫缝合技术与 CSP 发生的关系有待进一步探讨。2 CSP 的临床表现CSP 的临床表现缺乏特异性,主要为停经后阴道流血,有时伴有下腹痛,有大约 30%的患者没有临床症状仅在超声检查时被发现。 也有部分患者初诊为宫内早孕、难免流产或不全流产,在行人工流产术、药物流产或清宫术过程中出现大量阴道流血时才被诊断。 仍有大约 25%的患者因没有临床症状而未在早孕期被确诊。 当 CSP 未被及时诊断、严密监测或恰当处理时,可发生大出血、子宫破裂等严重并发症,导致失血性休克,甚至危及患者生命。
3 CSP 术中大出血的高危因素
探讨 CSP 术中大出血相关的高危因素有助于预测术中大出血的风险,并能指导临床分型诊断与治疗选择。 回顾性研究发现 CSP 术中大出血的危险因素包括妊娠次数多、孕周大、孕囊或包块较大、前壁肌层薄弱、 血人绒毛膜促性腺激素 ( humanchorionic gonadotropin, β⁃HCG) 水平高、孕囊周围血流丰富等。 不同研究分析得出的高危因素不尽相同,这可能与采用的治疗方式有关,但是多数研究均支持前壁肌层厚度及孕囊大小是预测术中大出血的重要提标。 Ban 等通过多因素 Logistic 回归分析发现,瘢痕处肌层厚度( OR:0.51,95% CI:0.36~0.73) 与 孕 囊 或 包 块 平 均 直 径 ( OR: 1.10,95%CI:1.07 ~ 1.14)是 CSP 术中大出血的独立危险因素,提示其可作为治疗方式选择的重要依据。
4 CSP 的诊断
超声检查,尤其经阴道超声,被认为是诊断CSP 的首选方法。 经阴超声不仅可以明确妊娠囊的位置、大小、瘢痕处肌层厚度、周围血流情况,还可以判断子宫瘢痕处是否外凸及与膀胱的关系。 经阴联合经腹超声可全面评估子宫的轮廓、是否外凸以及与膀胱的关系,有助于提高诊断率及进 行 临 床 分 型。 典 型 的 经 阴 道 超 声 表 现 为:①宫腔及宫颈管内未见妊娠囊;②妊娠囊着床于子宫瘢痕处肌层,部分可见胚芽或胎心搏动;③妊娠囊与膀胱之间的子宫前壁肌层明显变薄甚至连续性中断;④彩色多普勒血流显像( color dopplerflow imaging, CDFI)显示妊娠囊周边有丰富血流山东省医学会计划生育分会.剖宫产子宫瘢痕妊娠实用临床分型诊治专家共识 3信号,甚至呈现高速低阻的血流信号。 经腹超声矢状位图像发现子宫下段膨隆外凸,则有助于 CSP 的诊断。 当然,并非所有 CSP 的超声表现均符合上述所有的典型特征,部分患者的孕囊可能紧邻瘢痕处或血流稀疏。
经阴道超声诊断CSP 的最佳孕周是 6 ~ 7 周,随着孕周的增加,诊断难度增加,临床分型也可能随之改变,因此必要时需要动态监测来进一步评估。三维超声能够呈现出瘢痕处妊娠囊的立体图像准确位置及与瘢痕的关系,还可清晰显示前壁瘢痕处肌层厚度及子宫膀胱界面,从而有助于提高早期胎盘植入的检出率。 因此,三维超声是二维超声的有效补充手段,有助于提高 CSP诊断的准确性。 但目前尚不建议将三维超声作为 CSP 的常规检查。MRI 软组织分辨率高,能够明确妊娠囊与瘢痕的关系,客观测量瘢痕处肌层的厚度,有助于判断妊娠囊与膀胱的关系,对于 CSP 的诊断及分型具有重要的价值,是超声检查的重要补充手段。 MRI 尤其适于诊断困难或者高风险类型的患者,有助于指导治疗方案的选择。 但因 MRI 费用较高,且不适合动态监测,故不推荐作为常规检查和分型的依据。
血清 β⁃hCG 升高是诊断 CSP 的必要条件,对于CSP 的诊断及严重程度判断并无特异性,但在治疗后随诊评估中具有重要价值。 若发现血 β⁃hCG 异常升高或下降不满意,需要警惕瘢痕处妊娠滋养细胞疾病的可能。 另外,CSP 还需要与宫颈妊娠、宫内妊娠难免流产、不全流产、其余宫体瘢痕部位肌壁间妊娠等疾病进行鉴别。典型的超声表现同时结合剖宫产史、血 β⁃hCG升高即可诊断为 CSP。 及时、准确、详实的超声检查至关重要,有助于确定临床分型,以指导选择最佳的一线治疗方案。 值得注意的是,超声诊断存在一定的主观性和局限性,建议由经过专业培训的、经验丰富的妇科超声医生进行诊断,尽量提高超声诊断分型的准确性和同质化。 对于怀疑 CSP 而经阴道彩超不能确定诊断时,应联合 MRI 检查或及时转诊以尽快明确诊断,从而避免因延迟诊断或误诊导致严重并发症的发生。
5 CSP 的分型
越来越多的研究结果支持对 CSP 进行临床分型,并基于分型制定个体化的最佳治疗方案。 目前报道的 CSP 临床分型均基于超声检查结果。 2000年 Vial 等首次将 CSP 分为内生型与外生型,此分型方法简单易操作,已被国内外学者广泛应用。随着对 CSP 认知的增加, CSP 的分型也得到了进一步优化,综合妊娠囊位置、植入瘢痕处肌层的深度、周围血流情况及妊娠囊生长方向趋势等指标,对 CSP 进行了不同的分型。 这些分型系统有助于指导临床治疗,但超声诊断指标较宽泛,也未针对每种类型提供最佳的治疗方式选择,所以不能满足临床实际操作需要。山东大学齐鲁医院妇产科团队于 2015 年首次提出了瘢痕妊娠实用临床分型诊治策略(齐鲁分型)过回顾性病例分析,对原分型进行优化,提出新的临床分型诊治策略(齐鲁分型)。
此分型系统基于经阴道超声检查,根据 CSP 术中大出血的独立危险因素,即前壁肌层厚度与孕囊/ 包块大小的定量值进行分型,并针对每种类型分别推荐了最佳的一线手术治疗方案。 优点在于参照客观数据进行分型,量化标准,并依据分型指导临床治疗,便于临床医师掌握和实际操作。本共识推荐采用实用临床分型标准对 CSP 进行分型,分型标准及每种类型所推荐的最佳一线手术治疗方案见表 1,图 1。

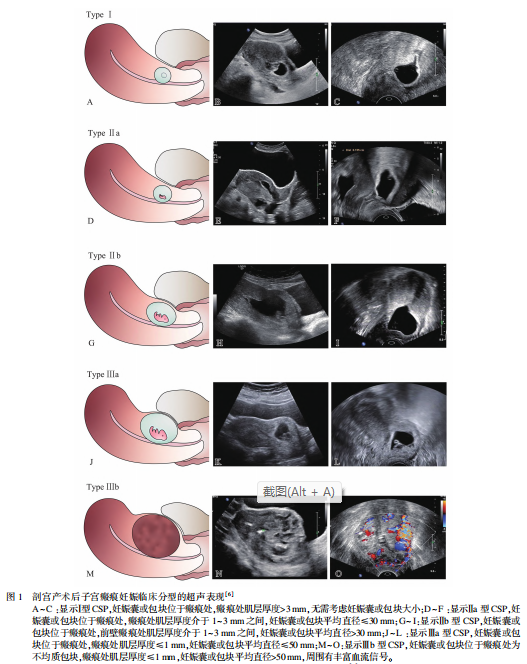
值得注意的是,每个病例的临床分型并不是一成不变的,若未得到及时治疗或治疗不当,其临床分型可由Ⅰ型转为Ⅱ型,甚至Ⅲ型。 因此强调早期诊断及初次恰当治疗的重要性。 对于重复性瘢痕妊娠的处理,也推荐参照此临床分型诊治策略。
6 CSP 的治疗
CSP 的诊治原则是早期诊断、准确分型、及时处理。 对于有剖宫产史的妊娠妇女,均要警惕存在CSP 的风险,建议于孕早期(6 ~ 7 周)尽早行妇科彩超检查,若发现存在 CSP,应同时明确临床分型。 除了少数强烈要求继续妊娠的患者外,对于大多数患者,建议积极进行干预性处理。 目前,CSP 的治疗方式多种多样,包括手术治疗、药物治疗、期待治疗及多种方法的联合应用,其中手术治疗还包括宫腔镜手术、腹腔镜手术、经阴手术、经腹手术以及子宫动脉栓塞(uterine artery embolizatiou, UAE)或高强度聚焦超声( high⁃intensity focused ultrasound, HIFU)预处理后手术治疗。 虽然治疗方式多样,但仍缺乏被广泛认可的国际和国内指南或共识指导。 选择一种安全、有效、经济的治疗方式的关键在于对病情的准确判断。 随着 CSP 治疗经验的积累,越来越多的研究支持基于临床分型来制定治疗方案,同时综合考虑有无胎心、出血风险、生育计划、医生诊治经验及医疗机构的资源来制定个体化治疗方案。 同时需要联合计划生育科、妇科、产科、超声科、介入科、麻醉科等多学科团队分析讨论,制定综合管理方案。
6.1 手术治疗
手术治疗是 CSP 的主要治疗方案,适用于没有继续妊娠意愿的所有类型患者。 治疗成功率最高,效果优于期待治疗和单纯药物治疗。Ban 等通过回顾性分析依据实用临床分型诊治策略处理的 564 例患者的临床资料,结果发现推荐的一线手术方案成功率达 97. 5%,其中微创手术占比达 96.1%,而需行 UAE 预处理的患者不足 1%,且无子宫切除术等严重并发症发生。 上述研究结果进一步验证了实用临床分型诊治系统治疗 CSP 的有效性及安全性。
该分型诊治系统既尽量采用了宫腹腔镜等最微创的手术方法,也避免了过度治疗,摒弃了传统的术前药物或 UAE 等预处理,避免了对患者生育力的影响。 并且,还可将患者进行很好的风险分层,将Ⅰ型及Ⅱa 型的低出血风险患者识别出来,留在基层医院进行处理,而高风险患者转诊至上级医院,以保障患者的安全,利于分级诊疗的实施,同时节约了医保费用支出。 该分型治疗体系优化了 CSP 的治疗模式,能够达到规范化、微创化、精准化及个体化治疗。 本共识推荐基于实用临床分型的个体化手术治疗方案策略,针对每种类型推荐最优的一线手术治疗方案,见图 2。
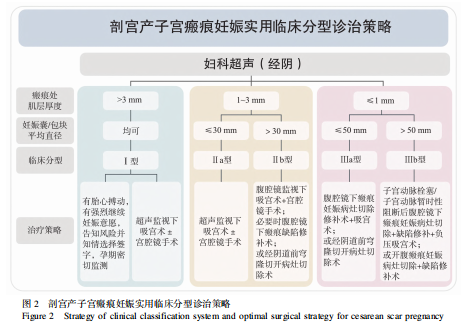
6.1.1 Ⅰ型 CSP 的手术治疗
对于Ⅰ型 CSP,推荐直接行超声监视下负压吸宫术±宫腔镜手术。 这种手术方式的优点是简单易操作、损伤小、恢复快、费用低;缺点是未同时行子宫瘢痕缺陷修补,瘢痕缺陷仍然存在。 因Ⅰ型患者直接手术出血风险低,不推荐药物等任何形式的预处理治疗。研究结果显示,超声监视下吸宫术±宫腔镜手术治疗Ⅰ型瘢痕妊娠的成功率达 98. 21% ( 165 /168) ,手术时间、住院时间及住院费用均低于其他类型的治疗方案。 多中心研究结果也证实对于Ⅰ型 CSP,超声监视下负压吸宫结合宫腔镜手术具有较高的成功率,优于单纯超声监视下负压吸宫术。超声监视不仅有助于探测宫腔避免子宫穿孔,判断妊娠组织是否清除干净,还可以监测有无继发性宫腔积血或宫壁局部血肿形成,可降低手术并发症风险,提高手术成功率。 宫腔镜可明确瘢痕处有无组织残留,尤其对于憩室较深或妊娠组织粘连、植入者,清宫术难以将组织完全清除,需要宫腔镜直视下评估有无胚物残留。 若发现有组织残留,可同时行残留组织电切术。
手术操作要点:①在扩张宫颈前,先经阴宫颈旁注射稀释的垂体后叶素 3~6 U,同时通知麻醉医师加强监护患者的生命体征;②负压吸宫时宜采用大吸管低负压进行,应先吸除子宫中上段及下段后壁的蜕膜组织,之后再以较小的压力吸除瘢痕处孕囊及蜕膜组织,尽量避免搔刮;③宫腔镜检查时要全面评估宫颈管、宫腔及瘢痕处形态及有无妊娠组织残留,着重检查瘢痕憩室的前壁及两侧壁;④若发现有妊娠组织残留,可先用电切环轻轻刮除,必要时再行组织电切,但应尽量避免电切过深,易导致子宫穿孔。 若术中出血多,或超声发现局部血肿持续增大,建议转为腹腔镜手术。
6.1.2 Ⅱa 型 CSP 的手术治疗
对于Ⅱa 型 CSP,推荐直接行超声监视下负压吸宫术+宫腔镜手术。 与Ⅰ型 CSP 比较,Ⅱa 型行单纯超声监视下吸宫术后妊娠组织物残留及出血的风险增加,因此需要加用宫腔镜手术,在直视下仔细评估有无组织残留,并同时行残留组织电切术。研究发现,对于Ⅱa 型患者,直接行超声监视下吸宫术+宫腔镜手术的成功率达 97.7%(166 / 170)。其中有 2 例患者因宫腔镜术中超声监视发现瘢痕处血肿形成,遂加做腹腔镜下瘢痕缺陷修补术,另有 2例患者因术后血 HCG 下降不满意,瘢痕处包块形成而再次入院治疗,1 例经药物治疗好转,另 1 例因包块较大伴有不规则阴道流血而行腹腔镜手术治疗。 宫腔镜术中应充分显露瘢痕憩室的顶部及两侧壁,评估有无组织残留,对于瘢痕憩室较深、顶部显露困难的患者,助手予下腹部耻骨联合上适当按压子宫下段,有助于更好的显露术野。 注意动作应轻柔,避免子宫穿孔,手术操作要点同Ⅰ型 CSP。
若术中出血多,或超声发现局部血肿持续增大,建议转为腹腔镜手术。对于Ⅱa 型患者推荐直接手术治疗,也不建议术前给予药物,UAE 或 HIFU 消融治疗等预处理。HIFU 消融治疗是将超声波聚焦于孕囊着床位置,通过超声波的热效应、空化效应、机械效应阻断瘢痕处浆肌层与孕囊之间的血流,以降低随后病灶清除过程中的出血风险。 虽然现有的临床研究结果已初步显示了 HIFU 在 CSP 术前预处理治疗中的安全性和有效性,但因 HIFU 费用较高,有腹痛等并发症,其临床应用价值及适应证优化选择需要更多的临床研究进一步探索。
6.1.3 IIb 型 CSP 的手术治疗
对于 IIb 型 CSP,推荐腹腔镜监视下吸宫术+宫腔镜手术,必要时加行瘢痕缺陷修补术;或者经阴道前穹隆切开病灶切除术。腹腔镜下配合负压吸宫术可快速清除瘢痕处妊娠组织,优点是微创,必要时可同时行瘢痕缺陷修补术。 手术操作要点:①经阴宫颈处注射稀释的垂体后叶素 3~6U 后,腹腔镜下充分下推膀胱返折腹膜,完全暴露子宫瘢痕部位,确定薄弱区的位置及情况;② 然后再于腹腔镜监视下行负压吸宫术,并用宫腔镜评估有无妊娠组织物残留;③如果术中发现瘢痕局部明显外凸、浆肌层菲薄、吸宫时明显下陷或术中出血多的情况,建议同时行腹腔镜下瘢痕病灶清除术+瘢痕缺陷修补术。 若术中出血多,应果断改行开腹手术。 建议手术由腹腔镜手术操作经验丰富的医师来完成。经阴道前穹隆切开病灶清除术的优点是微创、经济、手术时间短,可同时行瘢痕缺陷修补术,经阴道直视下缝合操作较腹腔镜下更清晰、容易、确切。
但是要求医师有丰富的经阴手术经验。 术前需要全面评估患者的情况,行妇科查体,评估有无阴道炎、阴道狭窄及宫体粘连情况,若发现阴道较窄,或子宫粘连于前腹壁宫体牵拉困难者,不适宜经阴手术。术前超声检查的评估也至关重要,测量病灶下缘距宫颈外口的距离,若>4 cm 者或病灶直径>6 cm 者,术中难以暴露病灶,也不建议经阴手术。 术中首先打开阴道前穹隆,分离膀胱宫颈间隙,暴露病灶,配山东省医学会计划生育分会.剖宫产子宫瘢痕妊娠实用临床分型诊治专家共识 7合负压吸宫清除宫腔内及瘢痕处妊娠组织,修剪瘢痕组织,缝合切口成形子宫。目前关于 CSP 术中同时行瘢痕缺陷修补是否能够增加再次正常妊娠率,降低重复性瘢痕妊娠的发生率,尚存在争议。 但是,对于有再生育要求、既往瘢痕憩室症状明显并希望同时修补子宫缺陷的患者,可积极行瘢痕缺陷修补术。
6.1.4 Ⅲa 型 CSP 的手术治疗
对于Ⅲa 型 CSP,推荐直接行腹腔镜下瘢痕妊娠病灶清除+瘢痕缺陷修补+负压吸宫术;或者经阴道前穹隆切开病灶清除术。 优点是直接行瘢痕处妊娠病灶切除,同时行缺陷修补术,术前不需要 MTX、UAE 等预处理。 与Ⅱb 型 CSP 策略不同的是,因瘢痕处肌层菲薄甚至缺失,需要同时行瘢痕缺陷修补术,一般不需要加用宫腔镜手术。腹腔镜下瘢痕妊娠病灶清除+瘢痕缺陷修补手术的操作要点:①经阴宫颈处注射稀释的垂体后叶素 3~6U 后,在腹腔镜下充分下推膀胱返折腹膜,完全暴露子宫瘢痕部位;②腹腔镜监视下行负压吸宫术;③打开瘢痕薄弱处肌层,快速彻底清除残留妊娠组织,注意瘢痕左右两侧角部的残留组织;④剪除菲薄或糟脆的瘢痕组织,切口连续缝合并水平褥式包埋,注意缝合两侧角部,避免过稀或者过密,成形子宫。 若术中出血多,果断改行开腹手术,不能一味追求微创而导致出血过多。 助手可使用 8 号吸引管适当举宫,利于下推膀胱及缝合操作。
6.1.5 Ⅲb 型 CSP 的手术治疗
对于Ⅲb 型 CSP,推荐 UAE 预处理后再行腹腔镜下瘢痕妊娠病灶切除术(患者无再生育计划),或腹腔镜下子宫动脉暂时性阻断后再行瘢痕妊娠病灶切除术,也可直接行开腹瘢痕妊娠病灶切除术。 对III 型瘢痕妊娠术中大出血高危因素的分析发现,妊娠囊/ 包块平均直径>5 cm 及伴有子宫动静脉畸形是两个独立的危险因素,若同时存在这两个高危因素,术中大出血的风险明显增加,推荐选择上述手术方式进行处理。 尤其对于经初次处理失败后的包块型患者,因绒毛植入肌层深、反复出血、感染等因素致组织糟脆,腹腔镜下不能短时间内清除妊娠组织,创面出血较多,推荐直接行开腹手术。 对于不合并子宫动静脉畸形的部分患者,也可行腹腔镜下瘢痕妊娠组织清除+瘢痕缺陷修补术,而不需要术前预处理,但须经过详细全面评估,由具有腹腔镜处理CSP 丰富经验的医疗团队实施手术。UAE 能够快速有效止血,常被用于难以控制的大出血时的急症止血治疗。
除此之外,UAE 还被用于 CSP 的术前预处理,能够减少术中大出血的风险,尤其适用于伴有动静脉畸形的Ⅲb 型患者的术前预处理。 建议于 UAE 预处理后 72 h 内行手术治疗。 研究报道,UAE 预处理后清宫与 MTX 预处理后清宫比较,在住院时间、术中出血量、血 β⁃hCG 恢复正常时间及不良反应等方面有优势。 UAE与其他手术方式联合应用,可增加 CSP 初治的成功率。 然而, 研究发现 UAE 对女性生育力有潜在的影响,可能导致卵巢功能下降、宫腔粘连、胎儿宫内生长受限、早产等并发症, 影响女性的生育力,因此对于有再生育计划或年轻的患者,不推荐选用UAE 治疗。
而且,UAE 费用较高,要求技术及设备条件较高,有动脉穿孔等并发症发生的可能。 因此,仅在有条件的医院,对患者严格评估后,方可谨慎选用 UAE。对于有再生育计划或年轻的患者,也可选择腹腔镜下子宫动脉暂时性阻断后再行瘢痕妊娠组织切除术,优点是避免 UAE 手术不良反应,保护患者生育力。 腹腔镜下在分离膀胱反折腹膜前,先行子宫动脉暂时性阻断,以减少病灶切除过程中的出血量。于骶韧带上 2 cm 处、输尿管外上方,打开阔韧带后叶,显露子宫动脉,予 1⁃0 可吸收线打活结以阻断子宫动脉血运,待病灶清除干净后,松开线结,观察无活动性出血后,再缝合关闭子宫切口。 腹腔镜下瘢痕妊娠病灶切除术的操作要点是先充分下推膀胱,然后配合负压吸宫术快速清除妊娠组织。 若术中出血多,及时转为开腹手术。开腹手术的操作要点:①术中应提前打开膀胱反折腹膜,充分下推保护膀胱避免损伤,完全暴露瘢痕处病灶;②于瘢痕处打开子宫肌层,快速彻底清除妊娠组织,同时注意清除宫腔底部蜕膜组织;③充分修剪瘢痕肌层,双层缝合子宫切口;④若术中出血多,可行双侧子宫动脉或髂内动脉暂时性阻断。IIIb 型瘢痕妊娠病情最重,术中大出血风险明显升高,需备足血源,不建议在基层医院处理,一旦诊断及时转诊至有经验的上级医院。
6.2 药物治疗
首选的治疗 药 物 是 甲 氨 蝶 呤 ( methotrexate,MTX), 但一般作为手术前的预处理, 不建议将MTX 单独用于 CSP 的治疗。 MTX 治疗 CSP 的适应证:①不愿意或不适合手术治疗的 CSP 患者,孕周越小,成功率越高;②手术治疗后有妊娠组织残留,血 β⁃hCG 水平下降缓慢,不适合短期内再次手术的患者。 且患者生命体征平稳,无 MTX 治疗禁忌证。MTX 可于孕囊局部注射,或肌注全身用药,也可联合 UAE(MTX 25 mg,分别双侧子宫动脉注射后栓塞,总量 50 mg)应用。 MTX 治疗期间,需定期监测妊娠病灶大小、血 β⁃hCG 水平变化,有无大出血以及子宫动静脉畸形形成,并应注意有无肝肾功能损伤等药物副反应,及时对症处理。 研究发现,与直接手术比较,MTX 预处理组住院时间长、后续清宫等手术时出血风险仍较大,且有一定的药物副反应。 因此,MTX 用于 CSP 术前预处理,并无明显优势。
6.3 期待治疗
对于初次治疗后瘢痕处胚物残留者,若瘢痕处包块较小,血 β⁃hCG 下降满意,阴道流血少,可选择期待治疗。 期待治疗过程中需要动态监测血β⁃hCG水平至正常,复查超声至包块消失,并随访阴道流血、腹痛及月经恢复等情况,并告知仍有大出血的可能。 若随访过程中发现血 HCG 下降不满意,包块呈增大趋势,或阴道流血较多的情况,需要给予药物保守或再次手术治疗。 尤其对于未行瘢痕缺陷修补的患者,术后有胚物残留、局部形成包块的风险较大,术后应加强监测。
6.4 瘢痕妊娠继续妊娠的管理
尽管建议 CSP 经确诊后尽早终止妊娠,SMFM指南也不推荐继续妊娠期待治疗,但临床上仍有少部分患者选择继续妊娠。 对于部分有胎心搏动的CSP I 型患者,若有强烈的继续妊娠意愿,可在严密监测下继续妊娠,但应充分告知相关风险并知情同意签字。 患者需具有良好的依从性,且具备良好的就医条件,至有处理 PAS 丰富经验的医院进行全程管理,联合多学科团队,动态监护下继续妊娠,于孕晚期早住院,剖宫产前做好应对抢救大出血及子宫切除的准备,方可获得较好的母儿结局。 继续妊娠过程中有出现大出血、PAS、子宫破裂甚至母胎死亡等严重并发症的风险,需严密监测,早期发现,及时处理。
一项综述总结了 17 项研究共 69 例行期待治疗的病例资料,发现在有胎心搏动组,有 13%(4 / 39)的患者发生了自然流产,其中 20%需要进行干预性处理,早中孕期子宫破裂发生率 9.9% (3 / 39)。 继续妊娠至晚期者占 76.8% (40 / 52),其中大出血发生率 29.6%(8 / 27),75%的患者伴有胎盘植入,子宫切除率达 15.2%(6 / 39)。 因此,对于有胎心搏动的 CSP 患者,选择继续妊娠期待治疗需要慎重。 对于 CSP 伴胚胎停育者,推荐按照临床实用分型诊治策略积极手术干预治疗,以避免严重并发症的发生。
7 CSP 治疗后的随访及生育规划
CSP 治疗后,需监测患者血 β⁃hCG 水平至正常,复查超声,随访阴道流血及月经恢复情况。 尤其对于未行瘢痕缺陷修补的患者,仍有绒毛残留、局部形成包块的风险,术后应加强监测,并告知仍有大出血的可能,必要时需要再次保守或手术治疗。对于术后 2 年内无再生育计划的患者,建议采用长效可逆的避孕方法,推荐宫内节育器或皮下埋植剂等。 对于有再生育计划,行瘢痕缺陷修补者建议严格避孕 1 年以上再妊娠,若未行瘢痕缺陷修补者需避孕半年后再次妊娠。 无论是否行瘢痕缺陷修补,再次妊娠时,仍有发生 CSP、胎盘植入、子宫破裂等并发症的风险,建议尽早行超声检查明确胚胎着床位置,并密切监测孕期情况。
 (1)
(1)
 (0)
(0)
