

1.0 PCOS的诊断
成人诊断
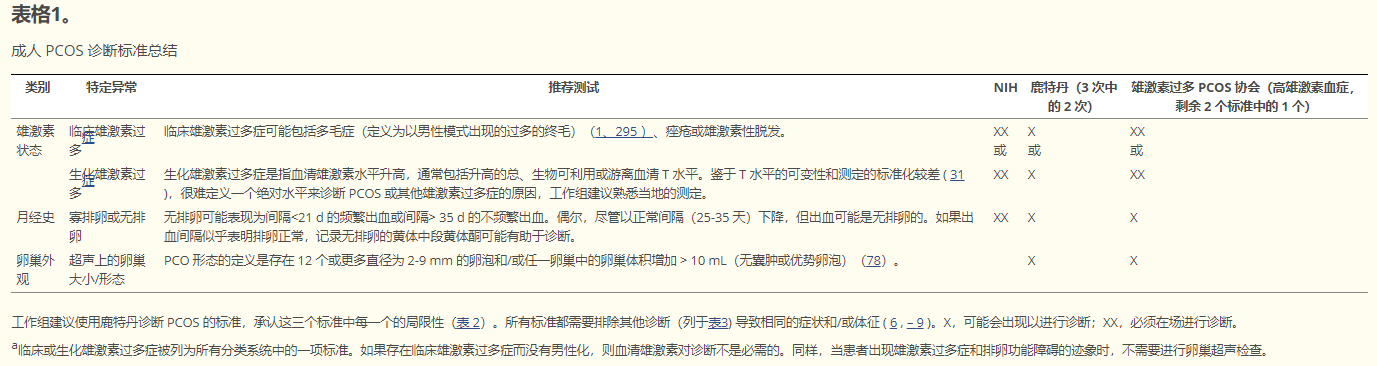
1.1 如果满足以下三个标准中的两个,我们建议诊断为 PCOS:雄激素过多、排卵功能障碍或 PCO(表 1和和2) ,2),而排除模仿 PCOS 临床特征的疾病. 这些包括,在所有女性中:甲状腺疾病、高催乳素血症和非典型的先天性肾上腺增生(主要是血清 17-OHP 导致的 21-羟化酶缺乏)(表 3)。在选择闭经和更严重表型的女性中,我们建议进行更广泛的评估,排除其他原因(表 4)(2|⊕⊕⊕○)。



1.1 证据
PCOS是一种具有全身代谢表现的常见疾病。其病因复杂、异质且了解甚少。目前使用的 PCOS 有三种定义,它们不同地依赖于雄激素过多、慢性无排卵和 PCO 来做出诊断(表 1)。然而,所有标准都是一致的,因为 PCOS 被认为是排除性诊断。所有三组诊断标准都包括高雄激素血症(临床或生化)和无排卵 ( 6 , – 9 )。鹿特丹标准是第一个将超声上的卵巢形态作为诊断标准的一部分 ( 8 , 9 )。
最近由美国国立卫生研究院 (NIH) 赞助的 PCOS 循证方法研讨会的专家组认可了鹿特丹标准,尽管他们确定了三个主要特征中每一个的优缺点(表 2)。这些标准允许临床诊断(基于高雄激素慢性无排卵病史)以及通过雄激素测定或卵巢超声检查进行生化诊断。如果患者在临床上已经满足三个标准中的两个,我们不赞成使用雄激素检测或超声进行普遍筛查。建议记录导致诊断的特征。我们建议使用鹿特丹标准的当前定义来记录 PCO 形态(至少一个卵巢有 12 个 2-9 mm 的卵泡或在没有 >10 mm 优势卵泡的情况下体积 >10 mL),在没有年龄的情况下- 基于标准。
模拟 PCOS 的疾病相对容易排除;因此,所有女性都应接受 TSH、催乳素和 17-OHP 水平筛查(表 3)(10 , – 12)。高催乳素血症可表现为闭经或多毛症 ( 13 , 14 )。甲状腺疾病可能表现为月经周期不规律。在雄激素过多症女性中,应排除非典型的先天性肾上腺增生,因为它可以在 1.5-6.8% 的雄激素过多症患者中发现 ( 15 , 16)。对于出现闭经、男性化或与 PCOS 无关的身体表现(例如近端肌肉无力(库欣综合征)或额叶隆起(肢端肥大症))的特定女性,应考虑并排除其他诊断(表 4)。
1.1 价值观和偏好
在缺乏基于证据的诊断标准的情况下,我们依赖于上述 NIH 专家组的建议。特定表型特征的存在可能导致不同的风险和合并症特征。例如,雄激素过多症可能与代谢异常高度相关,而月经不规则和 PCO 形态可能与不孕症高度相关。在解释已发表的研究时,临床医生应注意在进行研究时可能会使用与他们自己不同的标准。委员会指出,对于围初经期或围绝经期的女性,PCOS 的诊断存在问题,因为闭经和月经稀发是生殖成熟和衰老的自然阶段,循环雄激素和卵巢形态的变化也是如此。所以,我们在这些组中分别讨论 PCOS 的诊断。最后,由于有证据表明 PCOS 的遗传成分以及男性和女性亲属中生殖和代谢异常的家族聚集性,因此应仔细了解家族史,并考虑进一步筛查一级亲属。
青少年诊断
1.2 我们建议在存在持续性月经稀发的情况下,根据是否存在高雄激素血症的临床和/或生化证据(排除其他病理)来诊断青春期女孩 PCOS。无排卵症状和 PCO 形态不足以在青少年中做出诊断,因为它们在生殖成熟的正常阶段可能很明显 (2|⊕⊕○○)。
1.2 证据
所有 PCOS 诊断标准均针对成人(表 1)而非青少年。此外,正常的青少年生理可能会模仿 PCOS 的症状。月经稀发在正常青春期初潮后很常见,因此不是 PCOS 青少年特有的。无排卵周期占初潮后第一年月经周期的 85%,第三年占 59%,第六年占 25%。无排卵周期与较高的血清雄激素和 LH 水平有关 ( 21 )。大约三分之二的 PCOS 青少年会出现月经症状,三分之一的青少年会出现月经症状,范围从原发性闭经到频繁的功能失调性出血 ( 22)。因此,将持续性月经稀发或闭经评估为 PCOS 的早期临床症状是适当的,尤其是当它在初潮后持续 2 年时 ( 23 )。
痤疮很常见,尽管在青春期是短暂的(24);因此,不应单独使用它来定义青少年的雄激素过多症 ( 25 )。由于雄激素过多症的暴露时间较短,多毛症可能发展缓慢,因此在青少年中的严重程度低于成人 ( 26 )。然而,在一项研究中,多毛症是约 60% 青少年的主要症状 ( 27 ),并且可能提示青少年 PCOS ( 28 )。Ferriman-Gallwey 多毛症评分仅在成年高加索人中标准化,并且在青少年中可能具有较低的切点 ( 29 )。雄激素性脱发尚未在青少年中进行过研究,在诊断 PCOS 时应谨慎对待 ( 25 )。
在正常青春期成熟期间缺乏明确的雄激素水平截止点 ( 30 ),也缺乏 T 测定标准化 ( 31 )。此外,肥胖似乎会加剧高雄激素血症,因为与正常体重的女孩相比,相当大比例的肥胖女孩在青春期的雄激素水平升高(32)。青春期的高雄激素血症可能与晚年的不孕症有关 ( 33 ),在确定适当的青春期水平之前,应使用成人截止值。
最后,鹿特丹超声 PCO 标准未针对青少年进行验证。在该组中推荐经阴道卵巢超声会引起实际和伦理问题。经腹超声在评估卵巢方面已经受到限制,在技术上更不适合肥胖,这在青少年 PCOS 中很常见 ( 34 )。此外,多卵泡卵巢是正常青春期的一个特征,随着月经周期的开始而消退 ( 35 ),并且可能难以与 PCO 形态 ( 20 ) 区分开来。在这一人群中,升高的抗苗勒氏管激素水平可能作为 PCO 的无创筛查或诊断测试,尽管没有明确的临界值 ( 36 , 37)。
总之,青少年 PCOS 的诊断应基于完整的图像,包括雄激素过多的临床体征和症状、雄激素水平升高以及在月经稀发的情况下排除高雄激素血症的其他原因。
1.2 价值观和偏好
在提出这一建议时,委员会承认青少年 PCOS 的诊断不如成人简单。对有 PCOS 体征和症状(包括 PCOS 家族史)的少女进行全面的医学和实验室评估需要高度的认识。在获得更高质量的证据之前,该建议对早期诊断青少年 PCOS 以及时开始治疗具有更高的价值,这超过了误诊的危害和负担。
围绝经期和更年期的诊断
1.3 虽然目前还没有围绝经期和绝经期妇女 PCOS 的诊断标准,但我们建议 PCOS 的推定诊断可以基于生育年龄期间月经稀发和高雄激素血症的长期病史。超声上 PCO 形态的存在将提供额外的支持性证据,尽管这在绝经期女性中不太可能 (2|⊕⊕○○)。
1.3 证据
PCOS 从围绝经期到更年期的自然史研究很少,但该综合征的许多方面似乎有所改善。卵巢大小、卵泡计数和抗苗勒氏管激素水平(窦卵泡计数的标志)随着正常年龄的增长而降低,无论是否患有 PCOS ( 38 , – 40 )。然而,与正常女性相比,PCOS 女性卵巢体积和卵泡计数的下降可能较少 ( 39 , 41 , 42 )。同样,无论有无 PCOS 的女性,雄激素水平都会随着年龄的增长而下降(血清 T 在 20 至 40 岁之间下降 50%)(43,–45 ),有报道称 PCOS 患者的月经频率有所改善(46, 47 ),尽管几乎没有证据支持血清 T 下降与绝经过渡本身有关 ( 43 )。
绝经后妇女的 PCOS 诊断比青少年更成问题。诊断没有与年龄相关的 T 截止值。此外,用于诊断女性高雄激素血症的 T 测定不精确 ( 31 ),即使对于使用串联质谱技术的测定 ( 48 ) 也是如此。然而,支持性研究表明,有月经不规律史的 PCOS 女性的围绝经期和绝经后母亲往往具有 PCOS 的特征以及代谢异常,这意味着 PCOS 表型的某些方面可能会随着年龄的增长而持续存在 ( 49 )。非常高的 T 水平和/或男性化可能表明绝经后妇女存在产生雄激素的肿瘤。
1.3 价值观和偏好
我们认识到绝经后女性 PCOS 的诊断是有问题的,但认为如果女性早期没有症状,女性不太可能在围绝经期或绝经期患上 PCOS。我们认识到,很少有前瞻性研究记录 PCOS 女性卵巢功能随年龄增长的自然史。
2.0 相关的发病率和评估
皮肤表现
2.1 我们建议体格检查应记录 PCOS 的皮肤表现:终末毛发生长(见多毛症指南,参考文献1)、痤疮、脱发、黑棘皮病和皮赘 (1|⊕⊕⊕○)。
2.1 证据
雄激素过多症的主要临床表现包括多毛症、痤疮和雄激素性脱发。皮肤问题的病史应评估发病年龄、进展速度、以前的长期治疗(包括合成代谢药物)、治疗或体重波动的任何变化,以及皮肤问题相对于那些问题的性质其他家庭成员。在极少数情况下,可能会出现男性型秃顶、肌肉质量增加、声音变深或阴蒂肥大,这表明雄性激素水平和潜在的卵巢或肾上腺肿瘤或严重的胰岛素抵抗状态 ( 9 , 50 ) (表 4 )。值得注意的是,在患有 PCOS 的肥胖、胰岛素抵抗女性中,通常会出现黑棘皮病,皮肤标签也是如此。51 )。
多毛症
一般人群中多毛症的患病率在 5-15% 之间,根据种族和地理位置存在相关差异 ( 9 )。在一项针对临床雄激素过多症患者的大型研究中,950 名患者中有 72.1% 被诊断为 PCOS ( 16 )。因此,PCOS 代表了多毛症的主要原因,但多毛症的存在并不能完全预测排卵功能障碍。总体而言,大约 65-75% 的 PCOS 患者存在多毛症(尽管在亚洲人群中较低)(15 , 52)。多毛症可能预示 PCOS 的代谢后遗症 ( 53 ) 或不孕症治疗无法怀孕 ( 54 ))。腹部肥胖患者的多毛症往往更严重 ( 9 )。目视评估多毛症的最常用方法仍然是改良的 Ferriman-Gallwey 评分 ( 1 , 55 )。
痤疮和脱发
痤疮在患有 PCOS 的女性中很常见,尤其是在青少年时期,并且患病率各不相同(14-25%),与种族和患者年龄有关(56)。PCOS 中痤疮和多毛症的合并患病率仍然不明确,尽管有临床证据表明这些特征中的每一个的患病率都高于两者的结合 ( 57 )。雄激素性脱发可以通过众所周知的主观方法进行分级,例如 Ludwig 评分 ( 58 )。雄激素性脱发发生率较低且出现时间较晚,但它仍然是一个令人痛苦的主诉,伴有严重的精神病理合并症(9)。它可能与多毛症和痤疮有关,尽管与生化雄激素过多症相关性较差。一些研究表明雄激素性脱发与代谢综合征 ( 59 ) 和胰岛素抵抗 (IR) ( 60 , 61 ) 之间存在关联。一些研究发现,与多毛症相比,痤疮和雄激素性脱发并不是 PCOS 雄激素过多症的良好标志物 ( 53 , 62 )。
2.1 价值观和偏好
评估 PCOS 女性的多毛症、痤疮和脱发取决于仔细分级,但具有主观性。我们重视识别这些特别有压力的症状,即使它们与客观发现无关。脱发和痤疮可能与雄激素过多症有关,令人痛苦;因此,我们倾向于记录并考虑咨询皮肤科医生,并确定它们是否与脱发或痤疮的其他病因有关(如果对 HC 无反应)。需要更多的研究来量化高雄激素血症的皮肤症状与心血管疾病之间的关系。
不孕不育
2.2 患有 PCOS 的女性无排卵和不孕的风险增加;在没有排卵的情况下,不孕的风险是不确定的。我们建议使用所有寻求生育的 PCOS 女性的月经史来筛查排卵状态。一些患有 PCOS 和月经正常的女性可能仍会经历无排卵,黄体中段血清黄体酮可能有助于作为额外的筛查测试 (1|⊕⊕○○)。
2.3 我们建议在女性患有 PCOS 的夫妇中排除除无排卵之外的其他不孕原因 (1|⊕⊕○○)。
2.2–2.3 证据
不孕症是 Stein 和 Leventhal ( 63 ) 描述的 PCOS 的原始症状之一,并且是常见的主诉 ( 64 )。在大量出现 PCOS 的女性中,接近 50% 报告原发性不孕症,25% 报告继发性不孕症 ( 65 )。基于人群的不孕症研究表明,无排卵性不孕症(包括 PCOS)很常见,占病例的 25-40% ( 65 , 66 )。此外,据估计,PCOS 是排卵功能障碍的最常见原因,占排卵障碍的 70-90% ( 67 )。长时间无排卵可能与不孕症增加有关(68)。在一项将受试者随机分配至安慰剂或曲格列酮组的多中心试验中,患有 PCOS 的女性每月自发排卵率为 32%(69)。尽管如此,瑞典 PCOS 女性的终生生育能力与对照组相似,几乎四分之三的 PCOS 女性自然受孕(70)。
一些患有 PCOS 和月经正常的女性可能仍会出现无排卵,黄体中段血清黄体酮可能有助于作为额外的筛查测试。虽然不孕症的主要机制被认为是少排卵或无排卵,但还有其他潜在因素,包括卵母细胞能力下降 ( 71 , 72 ) 和阻碍植入的子宫内膜变化 ( 73 , 74 )。与 PCOS 相关的其他因素,如肥胖,也与生育力低下和受孕延迟有关 ( 75 )。还必须考虑男性因素不育或输卵管阻塞(PCOS 的一项研究发现,严重少精子症的发生率接近 10%,双侧输卵管阻塞的发生率接近 5%)(76 )。
2.2–2.3 价值观和偏好
在提出此建议时,我们强调 PCOS 和排卵功能障碍女性的不孕负担总体增加,尽管存在自发受孕,这可能会随着月经频率的改善和年龄的增长而增加。PCOS 女性的生育自然史以及缺乏排卵功能障碍的轻度表型的影响尚未得到很好的理解或描述。
妊娠并发症
2.4 由于 PCOS 女性因肥胖而加重妊娠并发症(妊娠糖尿病、早产和先兆子痫)的风险增加,我们建议对 BMI、血压和口服葡萄糖耐量进行概念前评估 (1|⊕⊕⊕○) .
2.4 证据
越来越多的证据表明 PCOS 对不良妊娠结局有影响。混杂因素包括诱导排卵导致的医源性多胎妊娠、不孕症治疗本身导致的妊娠并发症增加以及 PCOS 女性肥胖率较高。一些研究表明 PCOS 女性的早期妊娠丢失增加 ( 77 , 78 )。一项比较有和没有 PCOS 的女性的 IVF 结果的荟萃分析表明,两组之间的流产率没有显着差异(优势比 [OR],1.0;95% 置信区间 [CI],0.5-1.8)(79) .
PCOS 与妊娠糖尿病之间的联系最初是由回顾性数据提出的 ( 80 )。一项对 99 名患有 PCOS 的女性和 737 名对照组的研究指出,妊娠期糖尿病的发病率较高,但这主要是由于 PCOS 组的肥胖患病率较高 ( 81 , 82 )。相比之下,一项将 BMI 等混杂因素考虑在内的荟萃分析表明,PCOS 与妊娠糖尿病和高血压风险的增加独立相关(83)。这项荟萃分析表明,单胎早产(<37 周妊娠)与 PCOS(OR,1.75;95% CI,1.16-2.62)之间以及 PCOS 与先兆子痫(OR,3.47;95%)之间存在微小但显着的关联CI,1.95-6.17)。大多数报告高血压或先兆子痫与 PCOS 妊娠之间关联的研究规模较小且控制不佳,结果喜忧参半 ( 82 )。在一项规模最大的研究中,当控制未产(在 PCOS 中更常见)时,与对照妊娠(n = 737)相比,PCOS(n = 99)不是先兆子痫的显着预测因子(81)。尽管在病例和对照组之间仅注意到胎龄的绝对差异很小,但新生儿发病率却有所增加(83)。
2.4 价值观和偏好
在提出此建议时,我们认为应优先考虑减少妊娠并发症(如妊娠糖尿病、先兆子痫和 PCOS 女性早产)导致的总体发病率增加。这些增加的风险是由于 PCOS 本身还是与 PCOS 相关的特征(如 IR 或肥胖)需要进一步研究。
胎儿起源
2.5 宫内影响 PCOS 发展的证据尚无定论。我们不建议对 PCOS 女性的后代进行预防 PCOS 的具体干预措施 (2|⊕○○○)。
2.5 证据
非人类灵长类动物模型和绵羊模型表明,子宫内的雄激素暴露可能使胎儿在成年生活中表现出 PCOS 的特征 ( 84 , – 86 )。人类数据有限,但有证据表明,在患有典型肾上腺增生的女孩或患有男性化肿瘤的母亲中,雄激素对胎儿进行了编程(87、88)。患有 PCOS 的孕妇的雄激素水平可能会升高 ( 89 )。然而,一项针对 2900 名孕妇的澳大利亚研究表明,在 244 名 14-17 岁的女性后代中,妊娠 18 和 34 周的 T 水平与 PCOS 的存在之间没有关系(90)。PCOS 女性怀孕期间 T 水平与结局之间的关系仍有待使用准确的检测方法来确定。
有证据表明人类心血管疾病与宫内事件有关。宫内生长受限与冠心病、高血压和 T2DM 的发病率增加有关,为成人疾病的胎儿编程提供了证据 ( 91 )。有限的数据表明宫内生长受限可能与某些人群随后发生 PCOS 相关 ( 92 )。此外,部分小于胎龄儿出生的女孩有患肾上腺早发、IR 或 PCOS 的风险 ( 93 , 94 ),尽管这尚未在北欧的纵向人群研究中得到证实 ( 95)。现有数据支持出生后体重快速增加和随后的肥胖会加剧代谢异常和 PCOS 症状的概念 ( 94 , 96 , – 98 )。
子宫内膜癌
2.6 患有 PCOS 的女性有许多与子宫内膜癌发生相关的危险因素,包括肥胖、高胰岛素血症、糖尿病和异常子宫出血。然而,我们建议不要对患有 PCOS 的女性进行子宫内膜厚度的常规超声筛查 (2|⊕⊕⊕○)。
2.6 证据
PCOS 与子宫内膜癌之间的关联于 1949 年首次被描述 ( 99 )。很少有研究有足够大的队列来充分评估 PCOS 女性患子宫内膜癌的风险。在对英国 PCOS 女性的长期随访中,319 名女性与 1060 名对照女性的发病率数据超过 31 年。患有 PCOS 的女性没有更高的全因死亡率,但确实显示出子宫内膜癌发展的相对风险 (RR) 增加了 3.5 ( 100 )。最近一项评估 PCOS 与子宫内膜癌之间关联的荟萃分析表明,患有 PCOS 的女性患子宫内膜癌的风险增加(RR = 2.7;95% CI,1.0-7.29)(101),随后的系统评价证实了风险增加了 3 倍 ( 102 )。
子宫内膜癌流行病学中的几个因素表明与 PCOS 相关。患有子宫内膜癌的年轻女性更有可能是未生育和不育,多毛症的发生率更高,并且月经稀发的几率略高 ( 103 )。肥胖和 T2DM 常见于 PCOS 女性,也是子宫内膜癌的危险因素 ( 104 , – 107 )。在具有这些风险因素的女性中,体力活动得分低会进一步提高患癌风险 ( 108 )。
目前没有数据支持对无症状女性进行常规子宫内膜活检 ( 109 ) 或对子宫内膜进行超声筛查 ( 110 )。对无异常出血的女性进行超声筛查显示诊断宫内病变的准确性较差 ( 110 , 111 )。美国癌症协会不建议对处于平均风险或风险较高的女性(林奇综合征除外)进行子宫内膜癌常规癌症筛查,但应建议女性报告意外出血和出血点 ( 112 )。
2.6 价值观和偏好
在提出提高 PCOS 女性子宫内膜癌风险意识的建议时,特别是那些有异常子宫出血、长时间闭经、糖尿病和/或肥胖的女性,我们认为应该优先考虑子宫内膜癌发展的后果,这一优先级抵消了可用于与 PCOS 独立关联的有限数据。
肥胖
2.7 肥胖增加,尤其是腹部肥胖,与高雄激素血症和代谢风险增加有关(见心血管疾病预防指南,参考文献2)。因此,我们建议通过 BMI 计算和腰围测量 (1|⊕⊕⊕○) 筛查患有 PCOS 的青少年和女性是否增加肥胖。
2.7 证据
PCOS中肥胖的患病率
世界各地的肥胖患病率差异很大;然而,在肥胖背景率(30-70%)显着不同的不同国家进行的研究得出的PCOS患病率相似(52、113)。PCOS 的发病率是否可能与肥胖的日益流行平行尚不清楚,尽管据报道,随着 BMI 的增加,PCOS 的患病率呈现适度但不显着的趋势 ( 114 )。肥胖也可能聚集在 PCOS 家族中 ( 97 , 115 ),转诊到专科诊所的偏倚也可能增加 PCOS 与肥胖的关联 ( 116 )。
肥胖对 PCOS 表型的影响
一般肥胖和特别是腹部肥胖会导致相对高雄激素血症,其特征是 SHBG 水平降低和输送到靶组织的生物可利用雄激素增加 ( 117 , 118 )。腹部肥胖还与 T 产生率增加和脱氢表雄酮和雄烯二酮的非 SHBG 结合雄激素产生率有关 ( 119 )。PCOS 中的雌激素水平,尤其是雌酮水平也可能较高(120)。
当体重过重发生在青春期而不是婴儿期时,月经失调很常见(121)。在患有 PCOS 的成年超重和肥胖女性中,月经异常和慢性少排卵比正常体重女性更常见 ( 118 )。患有 PCOS 的肥胖女性对用于促排卵的药物治疗(例如克罗米芬、促性腺激素或脉动 GnRH)表现出迟钝的反应和较低的妊娠率(54、68、122)。
肥胖会增加代谢综合征、IGT/糖尿病 (DM)、血脂异常和 IR ( 118 , 119 , 123 , – 128 ) 的风险。纵向研究表明,IR 可能会随着时间的推移而恶化 ( 125 )。因此,肥胖的负面影响可能超过 PCOS 状态本身。
2.7 价值观和偏好
在提出这一建议时,委员会认为超重和肥胖可能对 PCOS 的早期发展和临床表现有重要影响 ( 93 , 129 , 130 )。从青春期到绝经后,肥胖的程度和分布可能会发生变化,应监测这些变化。
沮丧
2.8 我们建议根据病史对患有 PCOS 的女性和青少年进行抑郁和焦虑筛查,如果发现,提供适当的转诊和/或治疗 (2|⊕⊕○○)。
2.8 证据
基于社区和患者的小型观察性病例对照研究一致表明 PCOS 女性的抑郁症患病率增加。与非 BMI 匹配的对照组相比,PCOS 女性患者的自评问卷显示抑郁症状发生率增加 ( 131 , – 133 )。同样,在直接精神病学访谈的研究中,重度抑郁症发作和复发性抑郁症的终生发生率更高(OR,3.8;95% CI,1.5-8.7;P = .001),有七次自杀未遂史PCOS 病例与对照组相比高出134倍。在一项检查抑郁评分变化的纵向研究中,在 1-2 年的随访中,抑郁的发生率为 19%(135)。PCOS 女性中抑郁症和抑郁症状患病率的增加似乎与肥胖、雄激素水平、多毛症、痤疮和不孕症无关 ( 131 , – 133 , 135 , – 137 )。因此,使用不同患者组和识别方法对抑郁症的研究表明,患有 PCOS 的女性抑郁症患病率增加(138)。
基于社区和诊所的病例对照研究和使用精神病学访谈的研究表明,患有 PCOS 的女性患焦虑症和恐慌症的比率较高 ( 134 , 137 , 139 )。此外,饮食失调在 PCOS 女性中更为常见(OR,6.4;95% CI,1.3-31;P = .01)(132),包括暴食症(12.6 对 1.9%;P < .01) (133)。尽管许多患有 PCOS 的女性和青少年可能存在抑郁或焦虑病史,但对于那些没有事先诊断的人,使用 PHQ-2 等两项问卷的简单办公室筛查可能会有所帮助(140)。那些确定患有抑郁症或焦虑症的人应转诊接受进一步治疗。
睡眠呼吸障碍/OSA
2.9 我们建议筛查患有 PCOS 的超重/肥胖青少年和女性是否有 OSA 的症状,一旦发现,使用多导睡眠图获得明确诊断。如果诊断出 OSA,应将患者转诊至适当治疗机构(2|⊕⊕○○)。
2.9 证据
患有 PCOS 的女性患 OSA 的速度等于或超过男性。OSA 的高患病率被认为是高雄激素血症(PCOS 的一个决定性特征)和肥胖(PCOS 中常见)(141 , 142)的函数,尽管这些因素本身并不能完全解释这一发现。即使在控制 BMI 后,患有 PCOS 的女性出现睡眠呼吸障碍的可能性是对照组的 30 倍,出现白天嗜睡的可能性是对照组的 9 倍 ( 141 )。服用口服避孕药的 PCOS 女性似乎不太可能出现睡眠呼吸障碍 ( 141 ),这与接受激素替代疗法治疗的绝经后女性出现睡眠呼吸障碍的可能性较低一致(141)。143 )。最后,与体重匹配的对照组相比,患有 PCOS 的女性的平均呼吸暂停-低通气指数显着更高(22.5 ± 6.0 vs 6.7 ± 1.7;P < .01),在快速眼动睡眠中差异最为明显(41.3 ± 7.5 vs 13.5 ± 3.3;P < .01) ( 143 )。因此,肥胖带来的风险不足以解释 PCOS 中睡眠呼吸障碍的高发病率,这表明必须涉及其他因素。
PCOS 患者 OSA 的持续气道正压治疗在控制 BMI 后显示出适度改善的 IR ( P = .013) ( 144 )。在患有 PCOS 的年轻肥胖女性中,成功治疗 OSA 可提高胰岛素敏感性、减少交感神经输出并降低舒张压。这些有益效果的大小受持续使用气道正压通气的时间和肥胖程度的影响。
2.9 价值观和偏好
根据病史和身体检查或问卷调查很难诊断睡眠异常。多导睡眠监测应在经过适当认证的认证睡眠实验室进行。睡眠呼吸障碍/OSA 治疗的解释和建议应由董事会认证的睡眠医学专家做出。
NAFLD 和 NASH
2.10 我们建议了解 NAFLD 和 NASH 的可能性,但建议不要进行常规筛查 (2|⊕⊕○○)。
2.10 证据
NAFLD 的特征是肝脏中过多的脂肪堆积(脂肪变性),而 NASH 定义了 NAFLD 的一个亚组,其中脂肪变性与肝细胞损伤和炎症共存(在排除肝病的其他原因(病毒、自身免疫、遗传、饮酒、等). 原发性 NAFLD/NASH 最常与 IR 及其表型表现相关 ( 145 ). 超声记录的 NAFLD 在普通人群中的患病率为 15-30% ( 146)。与 PCOS 相关的危险因素包括年龄增长、种族和代谢功能障碍(肥胖、高血压、血脂异常、糖尿病)。由于许多 PCOS 女性存在代谢功能障碍,因此 PCOS 与 NAFLD 的关联并不令人惊讶,但现有文献,尤其是关于 NASH 风险的文献并不完整(147)。临床研究报告称,人群中 NAFLD 的患病率为 15-60%,这取决于用于定义肝损伤的指标(血清丙氨酸氨基转移酶升高或超声检查)、肥胖的存在和种族(147 , – 153)。雄激素过多是否可能参与 PCOS 女性 NAFLD 的病理生理学尚不清楚 ( 153 , – 155)。因此,可以使用肝功能障碍的血清标志物筛查患有 PCOS 和代谢危险因素和/或 IR 的女性。如果血清标志物升高,可以考虑通过超声和肝活检对纤维化进行无创定量 ( 156 )。
2.10 价值观和偏好
在提出此建议时,我们认为应优先确定患有 IR 和/或代谢综合征的 PCOS 女性的这种潜在主要并发症。然而,目前还没有简单可靠的 NAFLD 筛查试验,因为血清转氨酶升高的敏感性和特异性较低。我们还认为,与能够识别和应用 NASH 可靠标志物的胃肠病学家和肝病学家合作调查 NAFLD 的真实患病率应该是未来建议的研究重点。最后,虽然生活方式疗法、胰岛素增敏剂和抗氧化剂被认为是有益的,但目前还没有批准的药物来治疗 NAFLD。
2型糖尿病
2.11 我们推荐使用 OGTT(包括空腹和使用 75g 口服葡萄糖负荷的 2 小时血糖水平)来筛查患有 PCOS 的青少年和成年女性的 IGT 和 T2DM,因为她们患此类疾病的风险很高异常(1|⊕⊕⊕○)。如果患者不能或不愿意完成 OGTT (2|⊕⊕○○),则可以考虑 HgbA1c。建议每 3-5 年重新筛查一次,如果出现中心性肥胖、体重显着增加和/或糖尿病症状等临床因素,则建议更频繁地重新筛查 (2|⊕⊕○○)。
2.11 证据
患有 PCOS 的青少年和成年女性患 IGT 和 T2DM 的风险增加 ( 125 , 126 , 157 )。PCOS 的诊断使患 T2DM 的风险增加 5 到 10 倍 ( 125 , 126 , 157 )。美国多囊卵巢综合征女性和青少年的葡萄糖耐受不良总体患病率为 30-35%,2 型糖尿病患者占 3-10%。患有 PCOS 的非肥胖女性 IGT 患病率为 10-15%,T2DM 患病率为 1-2% ( 125 , 126 , 157 )。有限的研究表明,糖化血红蛋白检测 IGT 的敏感性较差 ( 158 , 159)。2 型糖尿病患者的一级亲属患 2 型糖尿病的患病率显着较高,证实家族史是一个重要的危险因素。多项研究还显示,随访期间葡萄糖耐量恶化 ( 126 , 158 , 160 )。
由于 PCOS 中 IGT 和 T2DM 的高风险,一些科学组织建议对患者进行定期筛查以检测早期糖耐量异常,尽管尚未指定筛查间隔 ( 161 , – 163 )。
2.11 价值观和偏好
在提出这一建议时,委员会相信 PCOS 与糖尿病之间紧密联系的证据强度,并认为通过早期诊断和治疗降低 IGT/糖尿病的发病率胜过筛查带来的任何不可预见的伤害或负担。我们推荐 OGTT 优于 HgbA1c,因为 IGT 与女性心血管疾病之间的相关性可能增加 ( 164 , 165 ),并且有可能在怀孕前识别出有妊娠 DM 风险的女性。妊娠早期患有 PCOS 和 IGT 的女性患妊娠期 DM 的风险更大(166),但目前没有足够的数据推荐对 PCOS 女性进行妊娠期 DM 的早期筛查。鉴于缺乏重新筛查理想时期的证据,我们武断地推荐了 3-5 年的时期。
心血管风险
2.12 我们建议对患有 PCOS 的青少年和女性进行以下心血管疾病危险因素筛查(表 5):早期心血管疾病家族史、吸烟、IGT/T2DM、高血压、血脂异常、OSA 和肥胖(尤其是腹部肥胖增加) ) (1|⊕⊕○○)。

2.12 证据
雄激素过多症和多囊卵巢综合征协会的成员进行了系统分析,并发表了关于评估 PCOS 女性心血管风险和预防心血管疾病的共识声明(167)(表 5)。除了甘油三酯升高和高密度脂蛋白 (HDL)-胆固醇降低外,PCOS 女性的低密度脂蛋白 (LDL)-胆固醇和非 HDL-胆固醇较高,而与 BMI 无关 ( 117 , 167)。患有 PCOS 的女性应在每次就诊时测量 BMI 和血压(如果非肥胖则考虑腰围;≥ 36 英寸为异常),在诊断 PCOS 后,额外的检测应包括完整的空腹血脂(总胆固醇、LDL-胆固醇、非高密度脂蛋白胆固醇、高密度脂蛋白胆固醇和甘油三酯)。
尽管高血压一直是一个不一致的发现,但患有 PCOS 的女性似乎处于危险之中,至少在以后的生活中是这样 ( 168 , – 170 )。尽管在许多研究中收缩压和舒张压均正常 ( 168 , – 171 ),但在其他研究中,与对照组相比,PCOS 女性的平均动脉压和动态收缩压升高 ( 172 )。此外,平均动脉血压的夜间下降较低,这一发现在患有 PCOS 的肥胖青少年中也得到了证实 ( 171 , 173 )。
PCOS 早期冠状动脉和其他血管疾病的解剖学证据已使用各种技术进行了记录。与年龄匹配的对照女性相比,PCOS 患者颈动脉内膜中层厚度增加是卒中和心肌梗死的独立预测因素(174)。动脉粥样硬化的另一个标志物,冠状动脉钙化,在 PCOS 女性中比在对照组中更常见,即使在调整了年龄和 BMI 的影响后 ( 175 , – 177 )。超声心动图揭示了 PCOS 女性和对照组女性之间的解剖和功能差异,包括左心房大小增加、左心室质量指数增加、左心室射血分数降低(178) 和舒张功能障碍 ( 179 , 180 )。值得注意的是,左心室质量指数与 IR 程度呈线性相关 ( 178 )。
 (1)
(1)
 (0)
(0)
